东南大学/华大合作发表最新Cell论文:实现器官发生早期完整胚胎的数字重建
来源:生物世界 2025-06-20 17:35
这些研究结果共同构建了一个单细胞分辨率的全面时空胚胎图谱,并辅以一个基于网络的探索工具,便于在胚胎的原生环境中导航空间基因表达和信号网络,为深入研究胚胎发育和疾病开辟了新途径。
胚胎发育包含一系列错综复杂且分层次的细胞命运转变,包括胚层形成以及随后的器官发生。在哺乳动物胚胎发育过程中,由原肠胚形成而来的三个胚层——外胚层、中胚层和内胚层相互协作,启动器官原基的形成。早期器官发生阶段尤为关键,它为器官的形成奠定了基础蓝图。这一阶段具有广泛的细胞命运程序化指定事件,并且对发育干扰的高度敏感性,使其成为研究正常胚胎发育和先天性畸形潜在机制的关键窗口。
2025 年 6 月 18 日,东南大学林承棋教授、华大生命科学研究院方晓东研究员、东南大学/南通大学罗卓娟教授、福建医科大学曹华教授、香港中文大学(深圳)刘瑾副教授作为共同通讯作者,在国际顶尖学术期刊 Cell 上发表了题为:Digital reconstruction of full embryos during early mouse organogenesis 的研究论文。
该研究在器官发生早期(E7.5-E8.0)以单细胞分辨率重建了完整的 3D “数字胚胎”,为早期器官形成提供了重要见解,也为研究发育和疾病提供了一个独特的空间平台。

早期器官发生是胚胎发育中的关键阶段,其特点是细胞命运的广泛确定以启动器官形成,但同时也具有较高的发育缺陷易感性。
在胚胎发育约第 7.5 天(E7.5)时,随着小鼠胚胎开始折叠,胚胎经历了其首次重大的形态转变,这一转变以诸如心管、原始肠管和头部褶皱等关键结构的出现为标志。在这个阶段,胚胎从数百个细胞迅速增殖到数万个细胞,而器官形成的复杂过程则依赖于细胞的精确迁移、定位和分化。这些事件受到时空基因表达模式和复杂信号通路的严格调控。然而,参与早期器官发生过程的细胞的确切空间起源仍在研究之中。
尽管斯佩曼组织者(Spemann organizer)在 1924 年就已被证实对外胚层的模式形成起作用,但在早期器官发生过程中控制中胚层和内胚层谱系的调控原则仍未得到解决。单细胞 RNA 测序(scRNA-seq)已成为一种强有力的工具,能够全面展现细胞类型组成、组织异质性以及发育过程中的基因表达情况。近年来,空间转录组学因其出色地能够解读区域化基因表达的能力而备受关注。然而,对整个器官甚至整个胚胎的空间转录组和细胞图谱进行重建仍是一项重大挑战。此外,在胚胎层面,细胞命运转变背后的信号网络在天然环境中的深入探索仍有待开展。
在这项最新研究中,研究团队将空间转录组学方法 Stereo-seq 与细胞分割技术相结合,对来自 6 个 处于器官发生早期的胚胎(E7.5-E8.0)的 285 个连续切片进行了分析,生成了器官发生早期整个胚胎的空间转录组图谱,其分辨率达到了单细胞水平。
通过开发可视化平台 SEU-3D,研究团队重建了 3D “数字胚胎”,能够精确反映原生胚胎环境中的基因表达模式和细胞状态。
在此基础上,研究团队绘制了内胚层和中胚层衍生物的空间细胞图谱,并揭示了复杂的跨胚层和细胞类型的信号网络。此外,研究团队还在 E7.75 的胚胎-胚外界面的前部确定了一个原基决定区(PDZ),揭示了在心脏原基形成过程中存在协调的信号交流。
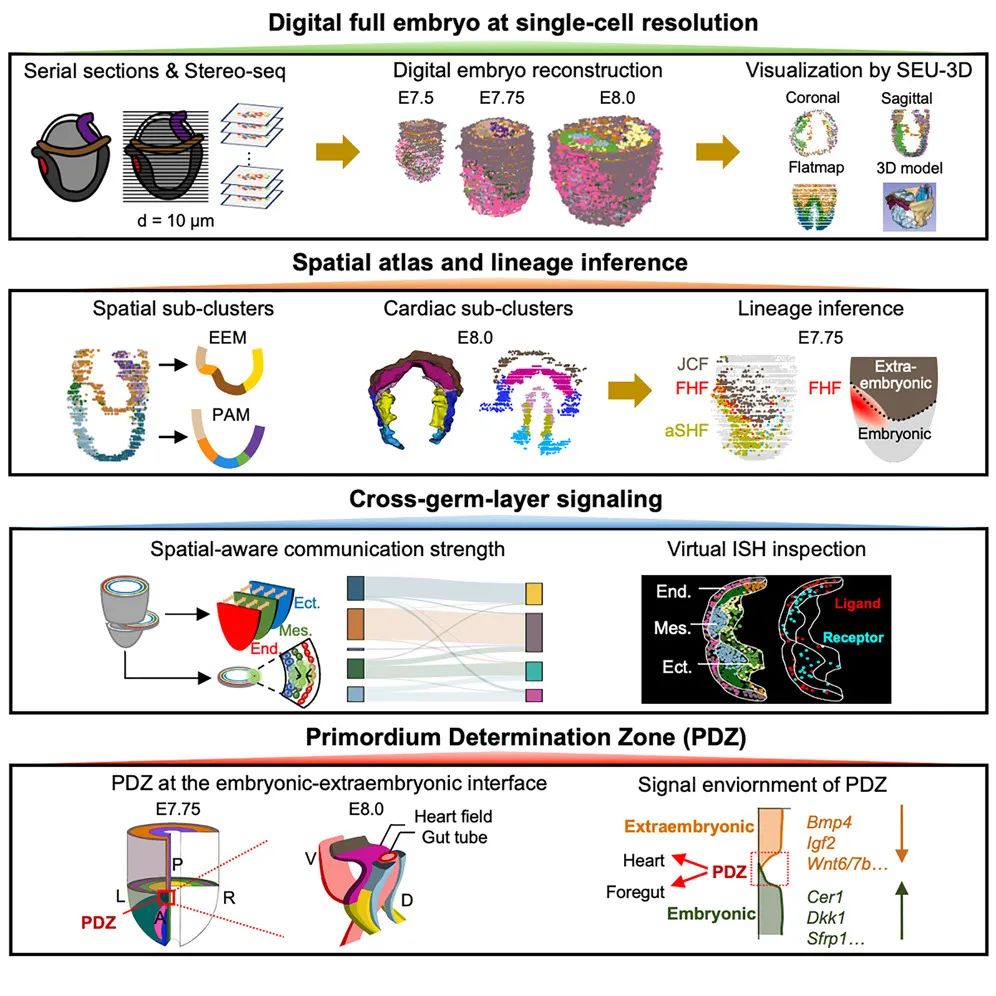
这些研究结果共同构建了一个单细胞分辨率的全面时空胚胎图谱,并辅以一个基于网络的探索工具,便于在胚胎的原生环境中导航空间基因表达和信号网络,为深入研究胚胎发育和疾病开辟了新途径。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


